L-酪氨酸作为多种高价值化学品的重要前体,在食品、医药和化工领域需求旺盛。尽管微生物细胞工厂为其生产提供了绿色可持续的途径,但其效率常受代谢途径固有复杂性和细胞生长与产物合成之间碳通量竞争的制约。本研究基于已建立的L-色氨酸生产底盘菌株,对莽草酸节点上游和下游的代谢通量进行了精细调控,并实施了辅因子循环驱动策略,使摇瓶发酵中L-酪氨酸滴度从2.5 g/L提高到8.6 g/L(提升3.4倍)。为解决生长-生产权衡问题,采用基于群体感应的动态控制策略调控TCA循环基因sucA的表达。进一步整合谷氨酸脱氢酶的筛选和强化,实现了细胞生长与L-酪氨酸生物合成的有效时空解耦。最终,工程菌株在5 L生物反应器中实现了81.3 g/L的L-酪氨酸滴度,细胞特异性生产力达到0.048 g/g DCW/h,创下了微生物L-酪氨酸生产的最高记录。本研究为芳香族氨基酸及其衍生物的高效可持续生物制造提供了有力策略。
关键词:L-酪氨酸、代谢通量、动态调控、细胞特异性生产力、生物制造
一、研究背景与意义
L-酪氨酸(L-Tyr)是一种重要的芳香族氨基酸,不仅是蛋白质生物合成的基本构建单元,也是多种高价值化合物的关键前体,在食品、医药和化工行业具有广泛应用。在食品工业中,L-Tyr广泛用作营养强化剂和功能性成分;在医药制造中,它是神经活性药物(包括多巴胺和左旋多巴)合成的重要前体;在化工领域,L-Tyr是合成酪醇、对香豆酸和咖啡酸等高附加值化学品的重要生物基原料。
随着应用领域的不断扩展,全球L-Tyr市场需求稳步增长。据市场分析,2024年全球L-Tyr市场规模约为15亿美元,预计到2030年将接近25亿美元,年复合增长率达7.2%。传统的L-Tyr生产主要依赖化学合成或蛋白质水解,这些方法往往操作复杂、原料成本高且环境负担重。相比之下,合成生物学和代谢工程的进展为微生物细胞工厂生产L-Tyr提供了更具成本效益和环境可持续性的替代方案。
当前研究挑战
尽管系统性代谢工程显著提高了微生物细胞工厂生产L-Tyr的生物合成能力,但实现工业化规模过程的严格要求(包括同时实现高滴度、高产率和高生产力)仍然具有挑战性。L-Tyr生物合成作为芳香族氨基酸途径的代表,本质上复杂,包含多个功能模块:莽草酸前体形成、芳香族氨基酸分支合成和辅因子生成。这些模块在碳通量需求、反应动力学和调控架构方面差异显著,系统性失衡已成为制约L-Tyr生物合成效率进一步提高的关键瓶颈。
二、研究策略与设计
Figure 1. 大肠杆菌中L-酪氨酸生物合成的系统性代谢工程策略。本研究中使用的基于QS的动态调控系统在大肠杆菌中生产L-酪氨酸的设计和策略。缩写:E4P:赤藓糖-4-磷酸;PEP:磷酸烯醇式丙酮酸;PYR:丙酮酸;DAHP:3-脱氧-阿拉伯-庚酮糖酸-7-磷酸;DHQ:3-脱氢奎尼酸;DHS:3-脱氢莽草酸;SHK:莽草酸;S3P:莽草酸-3-磷酸;EPSP:5-烯醇式丙酮酰莽草酸-3-磷酸;CHA:分支酸;PPA:预苯酸;4-HPP:4-羟基苯丙酮酸;L-Tyr:L-酪氨酸;L-Trp:L-色氨酸;L-Phe:L-苯丙氨酸;TCA:三羧酸循环;α-KG:α-酮戊二酸;L-Glu:L-谷氨酸。
本研究建立了一种系统性代谢工程策略,通过同时解决途径模块协调和细胞生长与产物形成之间的动态平衡来实现高效的L-Tyr生物合成。首先,强化L-Tyr生物合成途径内的关键节点,并精确调整莽草酸合成模块与下游莽草酸到L-Tyr转化模块之间的表达比例,以缓解模块间通量失衡。同时,通过增强NADH/NADPH辅因子相互转化来缓解各模块之间还原力供需不匹配的问题。
在这些静态优化基础上,实施了基于群体感应(QS)的动态调控策略,以实现对TCA循环中α-酮戊二酸脱氢酶(ODHC)活性的细胞密度依赖性控制,从而逐步将代谢通量从生物量形成重定向到产物生物合成。此外,引入了来自Salmonella enterica的谷氨酸脱氢酶,以加强α-酮戊二酸(α-KG)向L-谷氨酸(L-Glu)的转化,确保充足的氮供体供应和有利于L-Tyr生物合成的辅因子可用性。
三、L-酪氨酸生物合成途径的构建与优化
3.1 底盘菌株选择与L-Tyr途径重建
L-Tyr与L-色氨酸(L-Trp)和L-苯丙氨酸(L-Phe)同属芳香族氨基酸,其生物合成依赖莽草酸途径提供共同的芳香族前体。基于这种代谢相互依赖性,本研究选择实验室保存的L-Trp生产菌株TRP-12作为底盘菌株。该菌株在先前工作中经过系统性改造,主要聚焦于L-Trp生物合成途径,因此具有强大的芳香族前体供应能力。
然而,在TRP-12构建过程中,为最大化流向L-Trp的代谢通量,L-Tyr生物合成分支被有意破坏。具体而言,编码分支酸变位酶和预苯酸脱氢酶的tyrA基因从基因组中删除,导致L-Tyr生物合成途径不完整。为在TRP-12中重建L-Tyr生物合成,首先通过CRISPR/Cas9介导的基因组编辑恢复底盘菌株基因组中tyrA的表达。这一修饰重新连接了从分支酸到L-Tyr的分支途径,获得工程菌株TYR-0。摇瓶发酵实验表明,TYR-0能够合成并积累1.3 g/L的L-Tyr,证实了在TRP-12中重建L-Tyr生物合成途径的可行性。
考虑到L-Trp和L-Tyr分支之间潜在的代谢通量竞争,随后对L-Trp生物合成途径进行弱化以缓解这种竞争,同时维持正常的细胞生长。为此,采用起始密码子工程策略来调节L-Trp合成。具体而言,将L-Trp生物合成途径关键酶编码基因trpE的常规ATG起始密码子替换为效率较低的GTG起始密码子。这一修饰在不改变转录水平的情况下降低了翻译起始效率,从而适度减少了流向L-Trp生物合成的通量。结果,L-Trp积累从亲本菌株的5.4 g/L下降到工程菌株的0.35 g/L,证实了竞争L-Trp途径的有效弱化。所得菌株TYR-1在摇瓶条件下产生2.52 g/L的L-Tyr,相对于TYR-0提高了93.8%。
Figure 2. L-酪氨酸生物合成途径的构建和优化。(A) 菌株TRP-12、TYR-0和TYR-1摇瓶发酵过程中的L-酪氨酸和L-色氨酸浓度。(B) L-酪氨酸生物合成模块中关键靶点的摇瓶筛选。(C) 启动子工程实现aroL和aroA的平衡表达。使用不同强度的启动子:H,高表达强度(PJ23119);M,中等表达强度(PJ23108);L,低表达强度(PJ23114)。(D) 通过不同拷贝数质粒调控莽草酸模块和L-酪氨酸生物合成模块表达的L-酪氨酸生产优化。(E) 辅因子协调和优化策略示意图。(F) 辅因子工程菌株摇瓶发酵中的L-酪氨酸生产性能。
3.2 莽草酸节点上下游通量的协调
在以葡萄糖为唯一碳源的摇瓶培养条件下,菌株TYR-1能够产生L-Tyr,但发酵结束时培养液中检测到明显的莽草酸积累(约3.26 g/L),表明下游转化步骤存在代谢瓶颈。为确定限制从莽草酸流向L-Tyr的关键反应,系统评估了莽草酸到L-Tyr转化途径中涉及的多个候选限速酶。
单独过表达aroL或aroA使L-Tyr滴度从对照菌株TYR-1的2.52 g/L分别提高到3.64和3.40 g/L,对应1.44倍和1.35倍的提升。这一增加伴随着莽草酸积累的大幅减少。据此,aroL和aroA被确定为进一步组合优化的关键靶点。
使用pET28a作为表达载体,采用三种具有不同强度的组成型启动子(强PJ23119、中等PJ23108和弱PJ23114)独立调节aroL和aroA的表达水平。共构建了代表不同表达强度组合的9个质粒并导入菌株TYR-1,产生9个重组菌株TYR2-1至TYR2-9。摇瓶发酵分析显示,菌株TYR2-2实现了最高的L-Tyr滴度(5.7 g/L),而莽草酸积累显著降低至0.21 g/L。在该菌株中,aroL高表达而aroA维持中等表达水平。这些结果表明,aroL和aroA表达之间的适当平衡,而非统一最大化其表达,有利于莽草酸向L-Tyr的高效转化。
基于这种最优表达构型,将相应的aroL-aroA表达盒整合到菌株TYR-1的染色体中,构建基因组工程菌株TYR2。摇瓶发酵验证表明,TYR2保持稳定的L-Tyr生产,滴度达到5.92 g/L,比其前体菌株TYR2-2提高了0.22 g/L。这些结果共同证明,精细调节aroL和aroA的表达强度有效增强了从莽草酸流向L-Tyr生物合成的代谢通量。
3.3 模块化表达优化
值得注意的是,比较不同aroL-aroA表达强度组合的菌株发现,L-Tyr产量并未随下游生物合成模块更高表达水平而成比例增加。这一观察表明,仅通过强化下游途径表达无法进一步改善L-Tyr生物合成。在本研究使用的底盘菌株中,莽草酸前体供应模块已通过启动子调节进行工程改造,其中aroGfbr和aroE由强启动子(PJ23119)驱动,而aroD在相对较弱的启动子(PJ23114)下表达。这些结果共同暗示,需要协调调节莽草酸前体供应模块与下游aroL-aroA模块,以进一步增强L-Tyr生物合成性能。
因此,将工程化莽草酸途径视为一个整合的前体供应模块,并以模块化方式与L-Tyr生物合成模块协调调节。具体而言,将莽草酸供应模块和L-Tyr生物合成模块独立克隆到不同拷贝数的表达载体中,以调节每个模块的整体表达强度。采用低拷贝质粒pQJN、中拷贝质粒pEM和高拷贝质粒pCDR构建具有不同模块表达水平的模块化表达系统。通过组合配对不同拷贝数的载体,产生了9个具有差异化模块表达比例的工程菌株TYR3-1至TYR3-9。
摇瓶发酵筛选显示这些菌株之间L-Tyr产量存在显著差异。值得注意的是,当莽草酸供应模块从中等拷贝数载体表达而L-Tyr生物合成模块从高拷贝数载体表达时,菌株TYR3-4表现出最佳的整体性能,L-Tyr滴度达到7.8 g/L。
3.4 辅因子工程策略
为进一步增强碳通量并加速L-Tyr生物合成途径的整体运行效率,系统分析了莽草酸供应模块和下游L-Tyr生物合成模块的辅因子需求特征。这一分析揭示了两个模块之间还原力需求存在显著不对称性。具体而言,莽草酸供应模块内AroE催化的反应持续依赖NADPH,而在增强下游L-Tyr生物合成通量时,TyrAfbr催化的步骤不可避免地产生大量NADH。这些观察表明上游NADPH消耗与下游NADH积累之间存在内在失衡。
为强化细胞内从NADH到NADPH的转化,首先在菌株TYR3中过表达膜结合转氢酶pntAB,产生菌株TYR4-1,旨在全局性增加还原力再分配潜力。然而,摇瓶发酵结果显示单独过表达pntAB并未导致L-Tyr积累水平的显著提高。这一结果表明,在辅因子生成和消耗在空间上和功能上分布的代谢网络中,仅增强全局辅因子供应能力不足以维持途径特异性氧化还原反应的高效运行。
因此,提出了一种协同辅因子驱动策略,将辅因子再生直接与目标途径内关键还原反应相偶联。为此,将NADH生成酶TyrAfbr、转氢酶PntAB和NADPH依赖性酶AroE组装成单一表达模块并在菌株TYR3中共表达,产生工程菌株TYR4。这一设计通过局部NADH/NADPH同化将NADH生成与NADPH消耗功能偶联,建立了提供持续代谢驱动力的通路限制性交叉辅因子还原力循环。
摇瓶发酵表明,相对于对照菌株,TYR4的L-Tyr产量显著增加,滴度达到8.6 g/L。这些结果共同证明,将辅因子再生与限速氧化还原步骤协调偶联,而非非特异性增强全局辅因子供应,有效促进了目标途径内的还原当量周转,从而加速途径运行并将碳通量导向L-Tyr生物合成。
四、细胞生长与L-酪氨酸生产的智能调控
4.1 基于群体感应的动态调控系统
基于前述静态代谢工程策略,工程菌株表现出增强的L-Tyr生物合成能力。然而,在系统层面,L-Tyr生产仍与细胞生长紧密偶联,在几个关键代谢节点存在显著的通量竞争。其中,α-KG作为整合碳骨架供应、能量代谢和氮代谢的中心代谢枢纽,其流向下游TCA循环的通量分配直接与L-Tyr生物合成利用相竞争,导致生物量形成与产物合成效率之间的权衡。
为缓解这种通量竞争,实施了源自Pantoea stewartii的基于QS的动态调控策略,以细胞密度依赖性方式控制α-酮戊二酸脱氢酶复合物(ODHC)的活性。具体而言,动态调节ODHC的E1亚基(由sucA编码),以在早期发酵阶段维持正常细胞生长,随后在产物流阶段逐渐下调。
Figure 3. ODHC活性的动态调控改善L-Tyr生产。(A) 基于EsaI/EsaR的群体感应系统示意图。QS响应启动子PesaS的转录活性由转录调控因子EsaRI70V调控。在信号分子酰基高丝氨酸内酯(AHL)不存在时,EsaRI70V结合PesaS并激活下游基因转录。随着细胞密度增加,AHL的细胞内积累降低了EsaRI70V对PesaS的转录激活,导致PesaS控制基因在发酵后期表达降低。(B) 携带PesaS启动子控制下GFP的TYR5系列菌株的荧光光谱分析。(C) QS工程菌株TYR6-1至TYR6-4的摇瓶发酵性能。
为构建EsaI/EsaR-based QS调控回路,将转录调控因子基因esaRI70V和信号合成酶基因esaI整合到菌株TYR4的染色体中。esaRI70V基因置于组成型启动子PapFAB104控制下,以确保整个发酵过程中的稳定表达。
为实现对QS响应动力学的可调控制,系统调节esaI的表达水平以调节AHL合成速率。具体而言,esaI由一系列具有梯度强度的组成型启动子驱动(Pbs1-Pbs;强度:Pbs1 < Pbs2 < Pbs3 < Pbs),产生具有不同AHL积累特征的QS工程菌株TYR5-1、TYR5-2、TYR5-3和TYR5-4。
为表征QS调控的转录行为,将GFP报告质粒pET28a-GFP(其中GFP由QS响应启动子PesaS控制)导入这些菌株。结果显示,不同esaI表达水平的菌株表现出不同的GFP表达模式,随着AHL积累速率增加,GFP抑制的起始时间逐渐提前。这些结果表明QS系统提供了可调的、细胞密度依赖性的发酵过程中代谢通量控制。
在建立QS调控框架后,将菌株TYR5-1至TYR5-4中sucA的天然启动子替换为QS响应启动子PesaS,获得菌株TYR6-1至TYR6-4。摇瓶发酵结果显示,菌株TYR6-2在测试菌株中实现了最高的L-Tyr滴度(10.4 g/L),因此被选择进行进一步表征。
4.2 谷氨酸脱氢酶的强化
由于TyrB催化的转氨反应需要L-Glu作为氨基供体,如果QS介导的sucA抑制产生的α-KG不能有效导入谷氨酸合成途径,则其对L-Tyr生物合成的促进作用将有限。为强化这一代谢通道,分别过表达源自大肠杆菌、枯草芽孢杆菌和Salmonella enterica的谷氨酸脱氢酶(GDH),产生菌株TYR7-1、TYR7-2和TYR7-3。
比较发酵分析显示,来自S. enterica的gdhA提供了最有效的增强,使菌株TYR7-3的L-Tyr滴度提高到73.3 g/L。相应地,细胞特异性生产力提高到0.043 g/g DCW/h,表明L-Tyr生物合成的时空生产力进一步改善。这些结果表明,在强化GDH活性下,QS动态调控积累的α-KG被有效导入L-Glu生物合成,从而确保TyrB介导转氨步骤的充足氨基供体供应并增强L-Tyr生物合成途径的整体通量。
Figure 4. QS系统在5 L生物反应器中的放大验证和进一步优化。(A) 菌株TYR4和TYR6-2生物反应器培养过程中的细胞生长(OD600)曲线。(B) 菌株TYR4和TYR6-2生物反应器发酵中的L-酪氨酸滴度和产率。(C) 整合不同来源gdhA基因对菌株性能的影响。(D) 菌株TYR4和TYR7-3之间细胞内NADH/NAD+比率的比较。
进一步的细胞内辅因子分析显示,相对于无QS对照菌株TYR4,菌株TYR7-3表现出降低的NADH/NAD+比率。这一转变归因于ODHC活性的阶段特异性抑制,减少了TCA循环内的NADH形成并降低了细胞内NADH/NAD+比率。这种氧化还原转变有利于TyrA催化的NAD+依赖性催化步骤,从而促进高效的L-酪氨酸生物合成。
五、发酵放大与工艺优化
为提高菌株TYR7-3在生物反应器条件下的L-Tyr产量,在5 L搅拌釜反应器中系统评估了关键发酵参数。pH、接种量和溶解氧(DO)水平被选择进行优化,因为这些变量直接影响酶活性、细胞生理学和细胞内通量分布。
基线条件设定为pH 7.0、接种量10%(v/v)和DO水平20%。由于pH强烈影响发酵过程中的酶活性和代谢性能,首先考察了其对L-Tyr生产的影响。结果显示,在pH 6.4时获得最高的L-Tyr滴度,达到76.4 g/L,相对于基线条件提高了4.2%。
随后研究了接种量(10%、15%、20%和25% v/v)对发酵性能的影响。增加接种量导致最大OD600逐渐增加,表明生物量积累增强。相比之下,L-Tyr产量表现出非单调趋势,在接种量20%时达到最高滴度(77.2 g/L),相对于优化前条件提高了5.3%。进一步将接种量增加到25%使L-Tyr滴度降至69.2 g/L,表明过高的初始细胞密度促进碳通量分配向生物量形成而非产物合成。
在高细胞密度下,发酵后期的氧传递限制变得日益明显。为解决这一限制,通过调节通气速率和搅拌速度进一步优化DO控制,将设定点从20%提高到更高水平。结果显示,维持DO水平在40%使L-Tyr滴度达到76.9 g/L,证实了充足氧气供应在高细胞密度发酵中的重要性。相比之下,进一步将DO水平提高到50%导致L-Tyr产量降低,表明过高的氧气供应可能诱导不利的碳通量重分配。因此,选择40%的DO水平作为最优条件。
Figure 5. 5 L生物反应器中L-酪氨酸发酵过程的优化。(A) pH对L-酪氨酸生产的影响。(B) 接种量对L-酪氨酸生产的影响。(C) 溶解氧对L-酪氨酸生产的影响。(D) 菌株TYR7-3在最优发酵条件下的发酵参数。
综合优化pH、接种量和溶解氧,为菌株TYR7-3建立了稳健高效的发酵工艺。在优化条件下,5 L生物反应器中的补料分批发酵52 h实现了81.3 g/L的L-Tyr滴度、0.248 g/g葡萄糖的产率和0.048 g/g DCW/h的特异性生产力。这代表了本研究实现的最高时空生产力,证明了工程菌株和工艺的可扩展性和工业相关性,支持进一步的扩大开发。
六、文献报道的L-酪氨酸生产比较
Table 1. 文献中报道的微生物L-酪氨酸生产总结
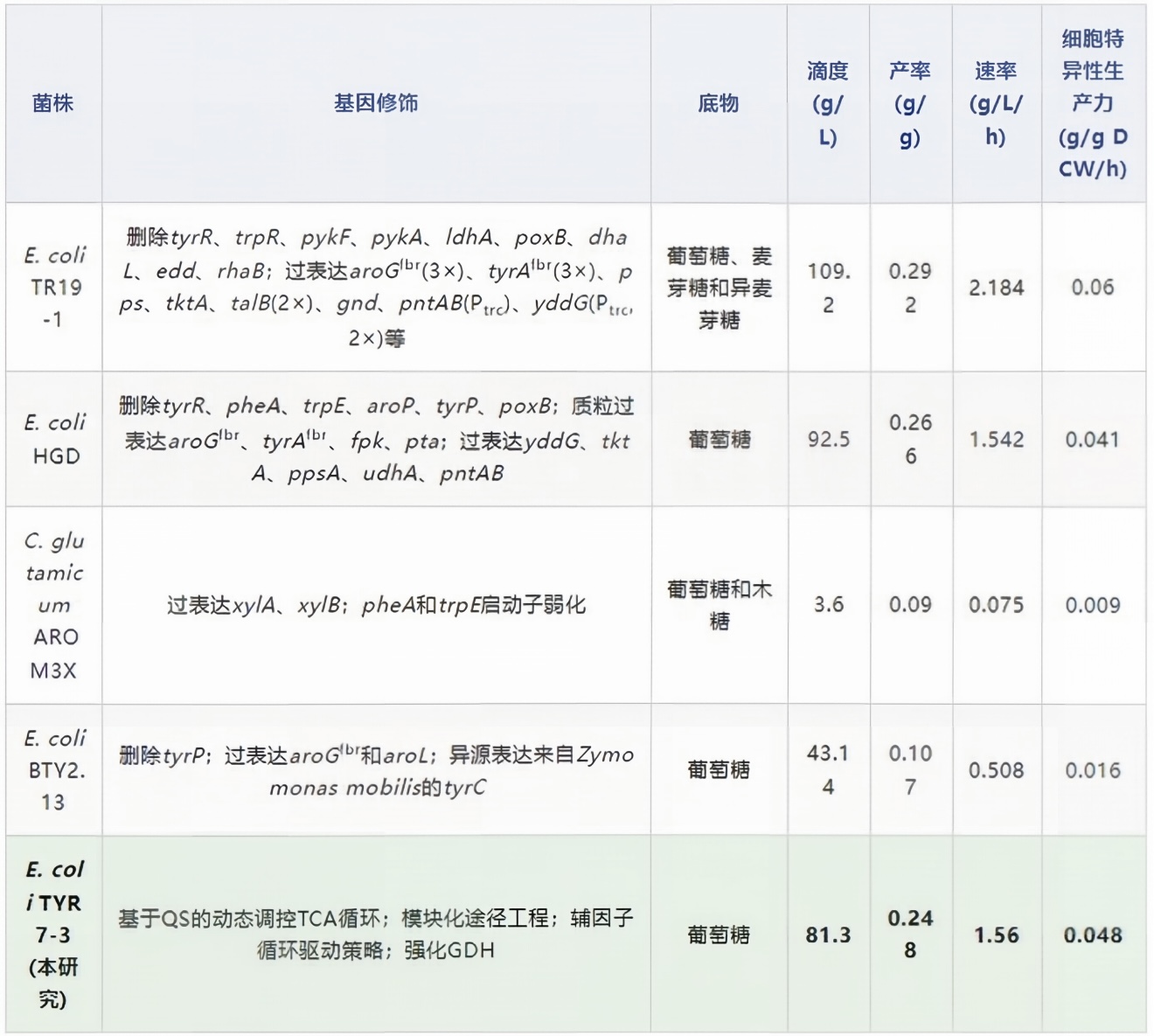
如Table 1所示,本研究获得的工程菌株TYR7-3以葡萄糖为唯一碳源实现了81.3 g/L的L-Tyr滴度,细胞特异性生产力达到0.048 g/g DCW/h。虽然E. coli TR19-1使用混合碳源实现了更高的滴度(109.2 g/L),但其细胞特异性生产力(0.06 g/g DCW/h)与本研究接近。值得注意的是,本研究实现了以葡萄糖为单一碳源的微生物L-酪氨酸生产的最高细胞特异性生产力记录。
七、讨论
本研究展示了一种整合代谢工程策略,通过将协调的途径模块化与细胞密度依赖性动态调控相结合来增强大肠杆菌中的L-Tyr生物合成。通过同时解决代谢网络的结构组织和代谢通量的时间分配,这种方法在保持稳健发酵性能的同时提高了单位生物量的L-Tyr生产效率。
7.1 模块化代谢工程框架
在大多数先前旨在提高L-Tyr产量的代谢工程努力中,优化策略主要集中于单个反应步骤或孤立的途径片段,如增强莽草酸积累或强化下游产物特异性生物合成途径。然而,L-Tyr生物合成跨越多个相互连接的功能模块,其上游莽草酸生产模块和下游L-Tyr形成模块在碳通量需求、反应动力学和辅因子需求方面存在显著差异。因此,孤立地放大单模块活性经常扰动内在代谢平衡,导致上下游通量不匹配、中间体积累或催化效率降低,最终制约整体途径性能的进一步提高。
为克服这些限制,实施了模块化代谢工程框架,将L-Tyr生物合成划分为以aroE、aroGfbr和aroD为中心的上游莽草酸生产模块,以及由关键节点aroL和aroA定义的下游L-Tyr形成模块。精细调节这些模块的相对表达水平和代谢负担,实现了上下游通量的协调匹配。重要的是,这些模块表现出不同的氧化还原需求:莽草酸生物合成中aroE催化的步骤需要持续的NADPH供应,而增强的下游L-Tyr通量通过tyrA催化的反应产生大量NADH。如果没有有效的氧化还原偶联或辅因子重分配,这种不对称的氧化还原需求代表了进一步通量放大的内在瓶颈。
通过整合tyrAfbr、pntAB和aroE,建立了两个模块之间的内部氧化还原偶联,其中L-Tyr形成过程中产生的NADH通过PntAB有效转化为NADPH并直接供应给NADPH密集型的aroE催化反应。这种辅因子连接通过同步碳通量与氧化还原来加速整体途径效率。值得注意的是,这一策略不依赖全局性增加还原当量库,而是在关键模块节点之间建立内在的氧化还原连接,从而促进平衡和协调的途径运行。
7.2 动态调控策略的优势
除途径水平优化外,细胞生长与产物形成之间的有效协调仍是进一步提高L-Tyr生产的核心挑战。以往的研究试图通过使用外部诱导型启动子、生长期响应元件或温控系统调控关键酶表达来解决代谢资源的阶段依赖性重分配问题。然而,这些方法通常需要额外的干预或复杂的工艺控制,限制了其稳健性和可扩展性。
特别是,基于温度的调控依赖发酵过程中的精确温度转换,对传热效率和反应器配置高度敏感,使放大过程中的可靠实施变得困难。生长期响应启动子可以部分反映细胞生理状态的变化,但其响应阈值和动态范围经常受宿主背景和培养条件的影响。类似地,外部诱导系统依赖化学诱导剂或人工干预,增加了生产成本并限制了其工业适用性,特别是在大规模发酵条件下需要生长和生产阶段之间稳定精确切换的情况下。
为克服这些限制,实施了基于QS的动态调控策略,以建立对中心代谢通量的自主、细胞密度依赖性控制。通过动态调节TCA循环关键节点α-酮戊二酸脱氢酶复合物的活性,该系统能够自动响应群体水平生理状态重分配碳通量。重要的是,调控时间与内源性细胞生长内在偶联,而非外部定义的控制点。这一设计消除了对外源诱导剂或复杂工艺干预的需求,同时确保生长阶段充足的能量和前体供应,并在生产阶段有效减弱向能量代谢的碳通量竞争。
7.3 研究局限性与未来展望
尽管静态途径优化与动态调控的协调整合显著改善了L-Tyr生物合成性能,但进一步改进的机会仍然存在。未来整合多组学分析的研究可能为模块间通量重分配和动态辅因子调控提供更深入的见解,从而实现更精确的调控靶点识别和调节。此外,将QS系统与额外的环境响应调控元件相结合可能进一步提高代谢效率。
从工艺开发的角度来看,在扩大培养和复杂原料条件下评估长期稳定性和性能对于工业转化至关重要。总体而言,本工作建立了芳香族氨基酸及其相关衍生物高效微生物生物合成的设计原则,并提供了一种广泛适用的策略,用于构建平衡高生产力与操作稳健性的细胞工厂。
研究结论
本研究通过系统性代谢工程策略构建了一株高效的L-酪氨酸生产菌株。途径模块协调与基于群体感应的动态调控相结合,实现了从生长到产物合成的代谢通量有效重分配。最终,在以葡萄糖为唯一碳源的条件下,工程菌株TYR7-3在52 h内实现了81.3 g/L的L-酪氨酸滴度,细胞特异性生产力达到0.048 g/g DCW/h,显著提升了L-酪氨酸生物合成的时空生产力。这些结果表明,将模块水平通量协调与内源信号驱动的动态控制相结合,为提高氨基酸生产的单细胞生物合成效率提供了一种有效且普遍适用的策略。
以上文章来源于微信公众号万物纯化。