一、中文标题
菌株开发与酶工程中的体内连续进化技术进展(Advances in in vivo continuous evolution technologies for strain development and enzyme engineering)
二、发表单位、通讯作者及发表时间
三、发表时间
发表时间:2026年4月
链接:https://doi.org/10.1016/j.biotechadv.2026.108895
四、科学问题
核心科学问题:如何克服传统进化工程中自然突变率低、体外突变文库规模小、表型筛选周期长等限制,通过体内连续进化技术实现快速、高效的菌株和酶性能提升?
关键挑战:
自然突变频率极低(每代约10⁻¹⁰突变/碱基),难以在可接受时间内产生显著表型多样化。
传统定向进化需反复构建和筛选突变文库,工作量大、耗时长。
多基因通路的同步优化面临组合序列空间爆炸性增长,缺乏高效并行手段。
五、摘要
进化工程是获得高耐受性、高产量工业菌株及高性能酶的关键策略,但自然突变率低、体外文库小、筛选周期长限制了其发展。体内连续进化技术通过在活细胞内实现诱变,提高突变率,使菌株或基因能够在数天至数周内完成自然条件下数十万至数百万年的进化。本文系统综述了基于易错DNA复制、DNA碱基修饰和DNA重组三大突变机制的体内连续进化平台。对每种机制,阐述了其设计原理、代表性应用、突变谱优化及筛选策略。通过比较其分子机制、优势和局限性,总结了该领域的最新进展,并展望了未来方向。本文为理解体内微生物连续进化技术提供了统一框架,并为菌株开发和酶工程提供了指导。
六、研究背景
在自然环境中,物种进化由随机突变与自然选择共同驱动。然而,工业微生物和酶通常需要远超其天然能力的性能。生产宿主必须被重新编程以强化生物合成途径、阻断副产物形成、增强辅因子供应并提高关键酶活性。由于我们对微生物代谢和酶结构-功能关系的理解尚不完整,理性遗传工程往往难以同时平衡细胞生长与产物形成,以及优化酶活性和稳定性。作为补充策略,进化工程在实验室条件下模拟自然进化,可弥补理性设计的不足。
根据进化目标,进化工程可在多个层面实施:(i)微生物的适应性进化;(ii)单个基因的定向进化;(iii)通路层面多基因的并行进化。然而,自然突变频率极低(约每代每10¹⁰个碱基发生一个突变),使得传统适应性进化缓慢且难以在可行时间内产生显著表型多样化。在酶工程中,定向进化通常需要大量人力和时间构建和筛选突变文库,文库规模受限于转化和筛选通量。在多基因通路层面,同时优化多个基因会急剧扩展组合序列空间,现有技术无法提供廉价、快速、大范围的并行表达修饰。
相比之下,体内连续进化技术将目标基因的突变率直接在活细胞内提高,实现突变群体连续、自主地产生,将自然条件下需数万至数百万年的进化时间压缩到实验室条件下的数天至数周,极大提高了传统进化工程的效率。基于突变机制,体内连续进化技术可分为三大类:(i)基于易错DNA复制的进化;(ii)基于DNA碱基修饰的进化;(iii)基于DNA重组的进化。本文系统总结了这三类技术的设计原理、优化策略及其在微生物细胞工厂开发和酶工程中的应用。
七、研究结果
结果1、基于易错DNA复制的进化技术
DNA复制由DNA聚合酶等酶系执行,校对功能保证了高保真性。通过突变校对结构域的关键残基,可将高保真聚合酶转化为易错变体,提高复制过程中的碱基错配频率。根据复制的遗传底物,分为三类:
1.1 宿主基因组复制型
通过改造复制性DNA聚合酶的校对亚基(如大肠杆菌DnaQ、结核分枝杆菌和谷氨酸棒杆菌的DnaE),实现全基因组范围的连续诱变。例如,携带校对缺陷DnaQ的大肠杆菌在1个月内即可分离出耐受1.25%正丁醇或乙酸胁迫下生长速率提高8倍的菌株。但全基因组诱变会积累大量中性或有害突变,需通过全基因组测序和反向代谢工程识别有益变异,耗时费力;同时突变率需低于致死阈值,平衡突变负荷与细胞活力具有挑战性。
1.2 靶向诱变系统
将易错聚合酶与CRISPR系统偶联,如EvolvR(nCas9融合易错Pol I),可在约350 bp窗口内产生所有12种碱基替换及短缺失。应用于鸟氨酸环化脱氨酶(OCD)进化,催化效率提高2.4倍。在酵母中开发的yEvolvR使ura3位点突变率提高约4个数量级。为扩大突变窗口,用高持续合成能力的T5/T7聚合酶替换Pol I,开发了CTRIE平台,窗口扩展至~2 kb,6天内使tatABC操纵子介导的周质蛋白分泌提高3倍。
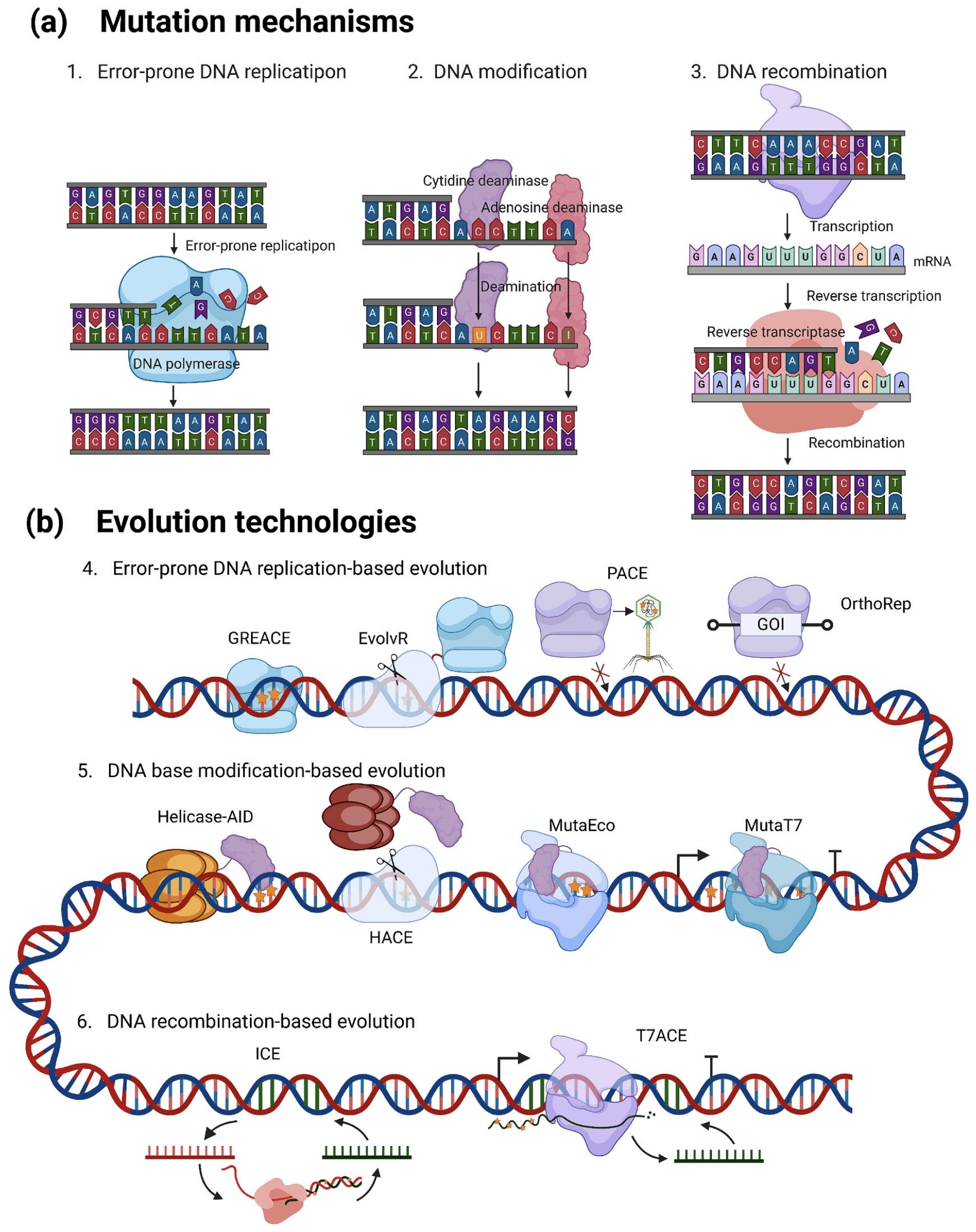
图1 体内连续进化机制
1.3 病毒复制型
将目标基因置于病毒基因组上,用易错聚合酶复制病毒,并将病毒增殖与目标蛋白功能偶联。最典型的是噬菌体辅助连续进化(PACE)。在PACE中,选择噬菌体(SP)的gIII基因被目标蛋白基因替换,而gIII由辅助质粒(AP)提供且其表达受目标蛋白活性调控。仅当目标蛋白活性提高时,噬菌体才能完成感染周期并被富集。PACE可在14天内完成约100轮蛋白质进化,已用于聚合酶、DNA结合蛋白、蛋白酶、碱基编辑器等的进化。衍生产品包括在哺乳动物细胞中的mPACE、植物细胞中的GRAPE,以及简化培养格式的SPACE(琼脂板上进行空间噬菌体辅助连续进化)。
1.4 质粒复制型
利用天然质粒(如ColE1、pGKL1/2、RSF1010)或人工构建的质粒(如TADR、BacORep、EcORep、T7-ORACLE)作为复制底物。其中,酵母中的OrthoRep系统利用Kluyveromyces lactis的线性质粒pGKL1/2,其编码自身专用的DNA聚合酶(TP-DNAP1),与宿主基因组复制正交。通过定向进化TP-DNAP1,质粒突变率提高至~10⁻⁴ substitutions per base,比基因组突变率高约10⁶倍,是迄今报道的最高突变率平台之一。OrthoRep已成功进化色氨酸合酶TrpB、嗜热HisA酶和氨酰-tRNA合成酶。最新开发的T7-ORACLE基于噬菌体T7复制机器,在大肠杆菌中实现质粒突变率~1.7×10⁻⁵ s.p.b.(比基因组高约10⁵倍)且无脱靶突变,同时满足高突变负荷和严格正交性。
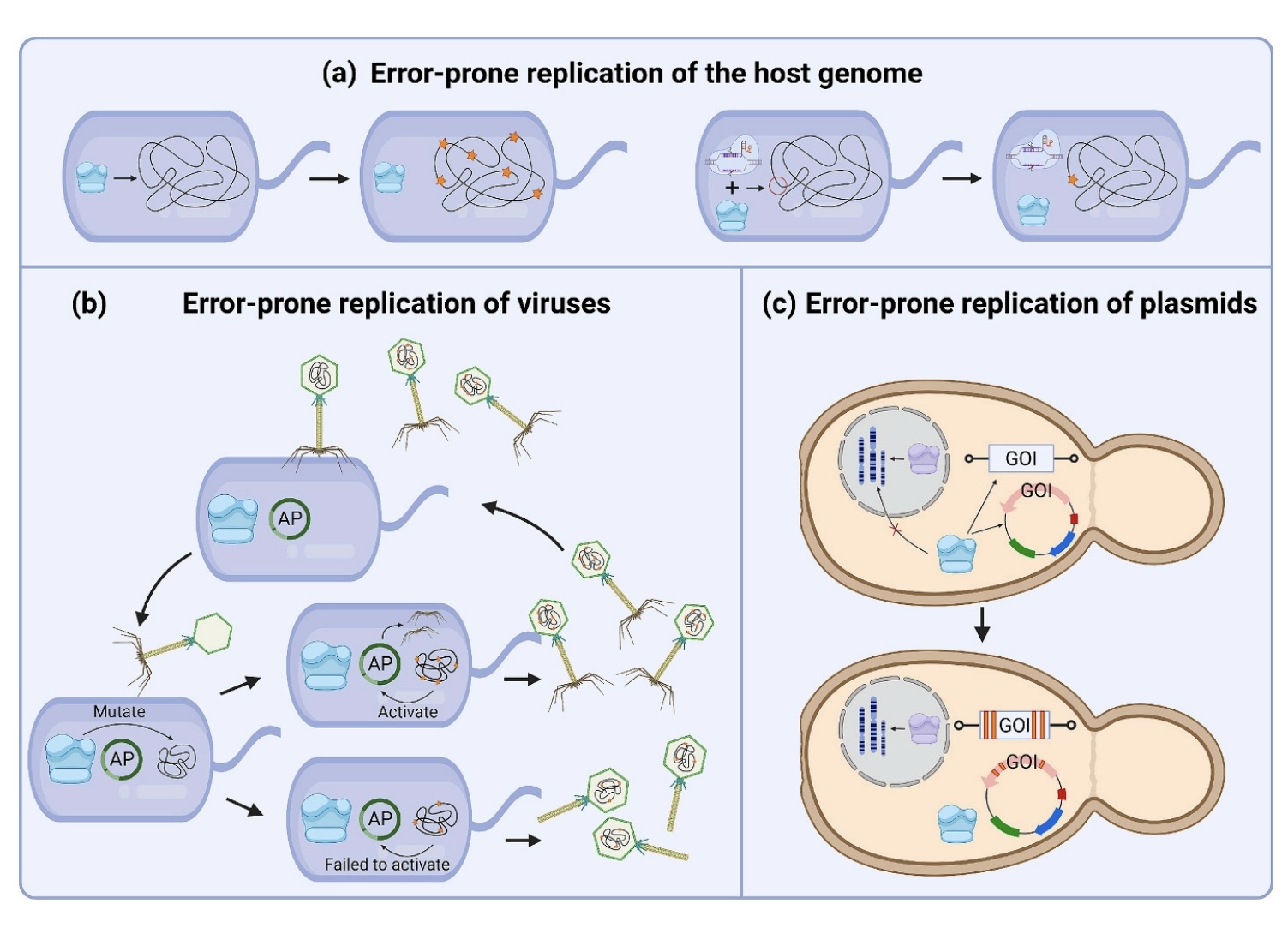
图2 易错PCR修饰
结果2、基于DNA碱基修饰的进化技术
DNA碱基修饰主要通过脱氨酶实现C→U→T和A→I→G转换。由于多数脱氨酶仅作用于单链DNA(ssDNA),需借助解旋酶或RNA聚合酶产生ssDNA。
2.1 解旋酶依赖型
将脱氨酶与复制性解旋酶(如大肠杆菌DnaB、RecQ;真核MCM5)融合,在复制叉处产生ssDNA并引入突变。例如,RecQ-AID在大肠杆菌中经4轮诱变使β-胡萝卜素产量提高371%;MCM5-AID在酿酒酵母和解脂耶氏酵母中分别使β-胡萝卜素产量提高75.4%和25%。修复相关解旋酶(如HACE系统)结合nCas9切口,可在~1000 bp窗口内连续诱变,已用于哺乳动物细胞中耐药突变的图谱绘制。双功能Cas3(I-E型CRISPR-Cas系统的效应蛋白)经灭活核酸酶结构域后与胞苷脱氨酶融合,开发了CoMuTER平台,在酵母中可靶向长达~55 kb的基因组区域(含4个基因的番茄红素途径),单轮诱变使番茄红素产量提高2倍以上。但CoMuTER仅产生C:G→T:A转换,突变谱窄。
2.2 RNA聚合酶依赖型
转录过程中RNA聚合酶会局部解开DNA双链形成转录泡,暴露ssDNA。基于此,将脱氨酶与T7 RNA聚合酶(T7 RNAP)融合,构建了MutaT7系列(MutaT7C→T、MutaT7A→G、MutaT7GDE)。通过优化脱氨酶(如eMutaT7)和削弱碱基错配修复,提高了突变效率。进一步将脱氨酶与宿主自身的RNA聚合酶融合,实现了全基因组进化:MutaEco(pmCDA1融合Eco RNAP)使大肠杆菌在1008小时内耐受8%乙醇;Mutator2(双功能脱氨酶CABE-T2.9融合)可同时引入C:G→T:A和A:T→G:C转换。但该类系统突变谱仍限于转换突变。
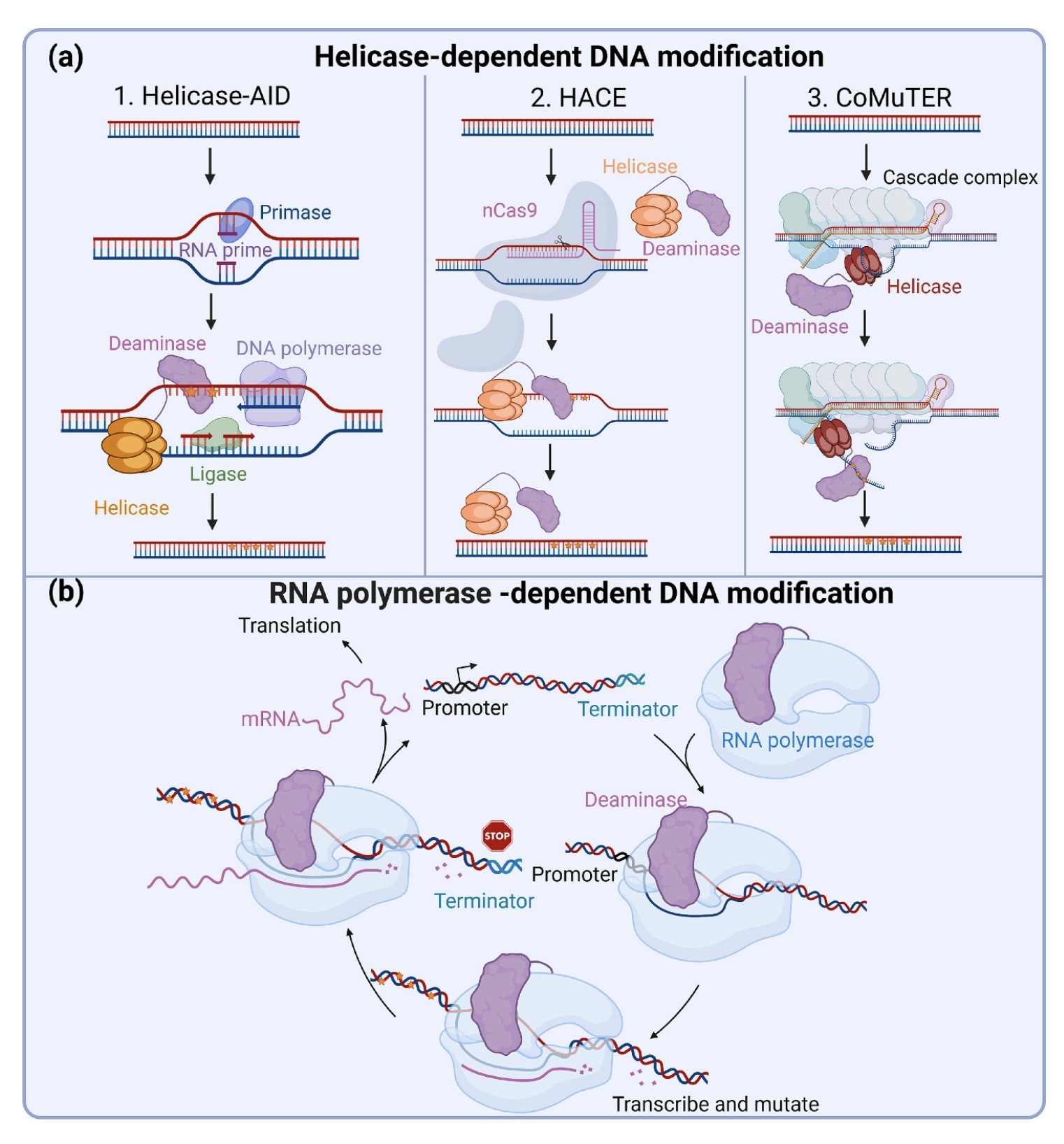
图3 DNA修饰
结果3、基于DNA重组的进化技术
3.1 位点特异性重组
Cre-loxP系统可诱导基因组发生缺失、重复、插入、倒位和易位。SCRaMbLE在合成酵母染色体中预装数千个loxPsym位点,诱导Cre表达后触发大规模重排,已用于提高乙酸耐受性和增强天然产物合成(如violacein产量提高3倍)。GEMbLER使用16种正交loxPsym位点独立重排启动子和终止子模块,单轮重组使虾青素产量翻倍。但此类技术需预先在基因组中安装重组位点,目前主要限于合成酵母。
3.2 ssDNA介导的重组
通过反转录酶或突变型T7 RNAP体内产生诱变的ssDNA,再通过同源重组整合到基因组中。ICE平台(酵母)利用Ty1反转录转座子,连续产生突变cDNA并重新整合,已用于进化URA3、转录因子Spt15(1.4%丁醇下生长提高44%)和木糖利用途径。REGES(大肠杆菌)利用retron编码的反转录酶,结合MutaT7产生突变RNA并反转录为ssDNA。T7ACE系统通过定向进化T7 RNAP使其能合成诱变ssDNA,在大肠杆菌和酵母中分别使靶基因突变率提高~2800倍和~1200倍,7天内使替加环素耐药性提高8倍、木糖利用效率提高2倍,窗口达~5 kb。该类技术的整体突变率通常低于复制型或修饰型系统,但可通过过表达单链退火蛋白(SSAPs)或敲除ssDNA外切酶(RecJ、SbcB)提高重组效率。
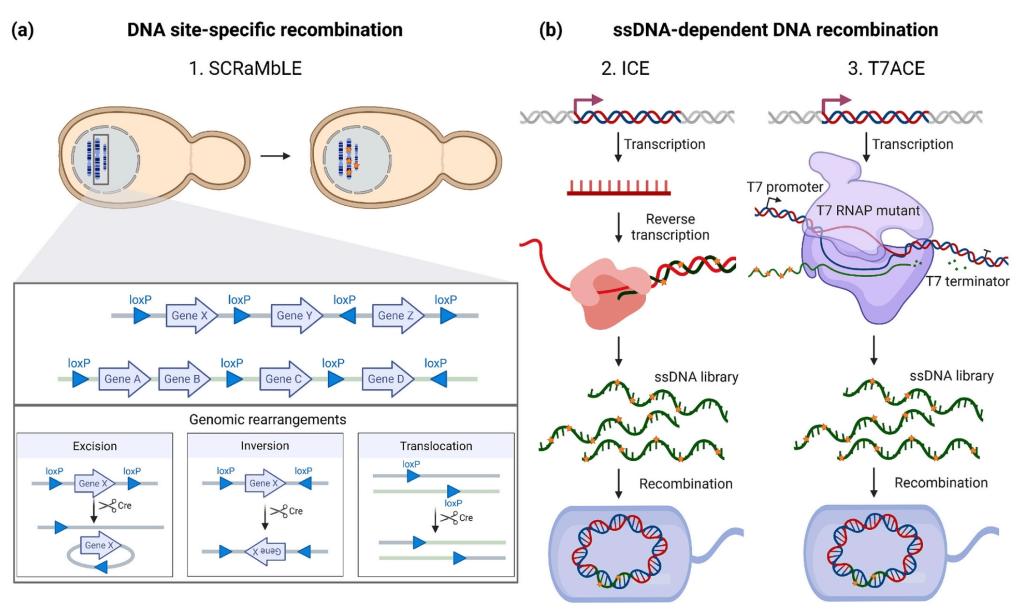
图4 DNA重组
八、讨论
本文系统综述了基于易错复制、碱基修饰和重组三大机制的体内连续进化技术。复制型系统突变谱最广(涵盖所有碱基替换类型),但设计难度大,且需平衡突变负荷与细胞活力;将诱变限制在噬菌体或正交质粒上可解耦突变负荷与宿主生存,成为当前研究热点。修饰型系统设计简单,但突变谱窄(主要为转换突变),虽已开发双功能脱氨酶,但仍不及复制型多样。重组型系统可大规模重塑基因组结构,潜力巨大,但受限于重组模块的可得性和构建复杂度。
未来方向包括:(i)结合人工智能设计更高活性、更宽突变谱的聚合酶、脱氨酶和重组酶;(ii)增强系统在非模式宿主中的兼容性和通用性;(iii)开发基于生物传感器的高通量筛选技术,结合自动化连续培养设备(恒化器、浊度计等),实现诱变-筛选-验证全流程自动化。体内连续进化技术正从概念验证走向工业应用,将极大加速高性能菌株和酶的开发。
以上文章来源于微信公众号合成生物智造。